

¿Sabías que los compuestos orgánicos que solo contienen carbono e hidrógeno se llaman hidrocarburos?



El carbono presenta propiedades químicas especiales que le permiten que sus átomos puedan unirse entre sí mismos formando infinidad de estructuras químicas cuyo arreglo geométrico puede ser lineal, ramificado o cíclico.
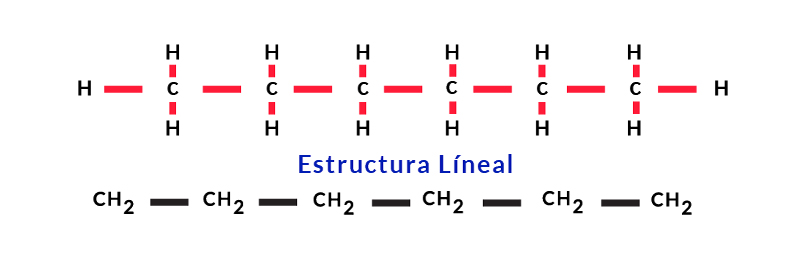
Los átomos de carbono se unen entre sí a través de enlaces covalentes sencillos, dobles, o triples.
También se puede unir con átomos de hidrógeno a través de enlaces covalentes sencillos; con el oxígeno, el carbono se une mediante un enlace covalente simple o doble y con el nitrógeno puede formar incluso un enlace covalente triple.


El carbono en el cuerpo humano representa el 18% de nuestra composición, la importancia de conocer la estructura del carbono y su habilidad de unirse consigo mismo y con otros bioelementos (hidrógeno, oxígeno, nitrógeno, azufre, fósforo), mediante enlaces químicos fuertes, es que éstos se combinan dando origen a una enorme variedad y cantidad de compuestos químicos, con diferentes propiedades, tales como las proteínas, los ácidos nucleicos, los carbohidratos, los lípidos y las vitaminas.
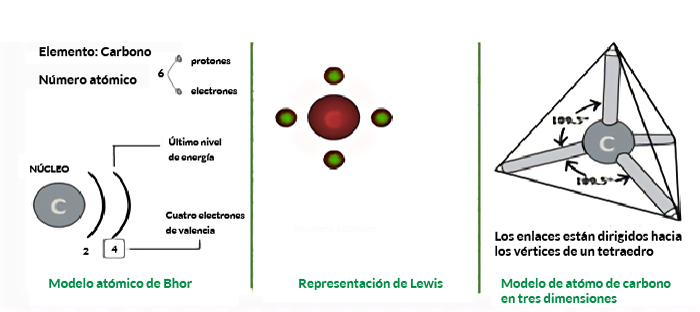
La estructura del carbono es tetraédrica, es decir que en su capa electrónica más externa (su órbita de valencia), tiene cuatro electrones de valencia que puede compartir, por lo que tiene la capacidad de formar cuatro enlaces covalentes con otros átomos de carbono o con átomos de otros elementos.
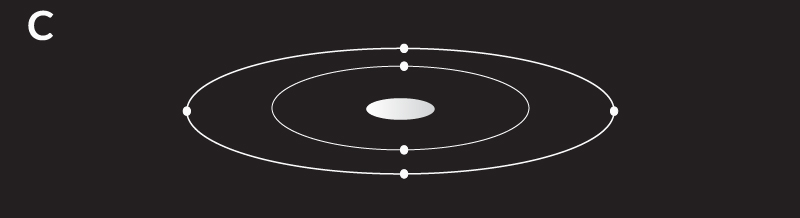
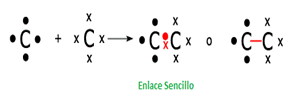
El esquema muestra el modelo atómico de Bohr en el que se visualizan los electrones de valencia que tiene el átomo de carbono.
Como podrás observar, cada átomo de carbono aporta un electrón para que se forme un fuerte enlace covalente simple o sencillo que resulta difícil de romper. Esto confiere gran estabilidad a la cadena de átomos de carbono frente a las reacciones químicas.

Las uniones C-C y C-H de las moléculas orgánicas son esencialmente no polares.
Estos factores estructurales le confieren muchas de sus propiedades a los compuestos orgánicos que forma. Por ejemplo, las moléculas relativamente no polares no se atraen con fuerza, lo cual afecta las temperaturas (puntos) de fusión y ebullición que suelen ser menores de 400° C. Otra propiedad es la baja solubilidad de los compuestos orgánicos en agua.

Enseguida te presentamos un ejemplo: en la molécula de etino o acetileno, los dos átomos de carbono forman un triple enlace porque se comparten tres pares de electrones.

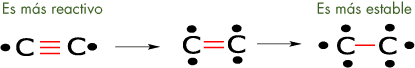
Un hecho importante que debes observar es que la fuerza de atracción de los átomos sobre los electrones que forman el doble o triple enlace es menor que la que ejercen sobre los electrones que forman el enlace simple.
A esta propiedad se le atribuye que los compuestos que contienen dobles o triples enlaces sean más reactivos, es decir son más débiles, que los que tienen enlaces simples.

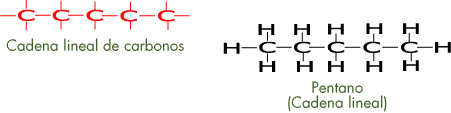
Llegó el momento de hacer una síntesis de las propiedades más importantes del átomo de carbono:.

Responde el siguiente cuestionario seleccionando la respuesta correcta.
Recuerda que el carbono tiene en su última capa de valencia 4 electrones para compartir.
Recuerda que el enlace covalente no polar es característico de las moléculas orgánicas.
Recuerda que el enlace que se forma entre un átomo de hidrógeno y uno de carbono siempre es sencillo.
Recuerda que los enlaces sencillos son menos reactivos y por tanto más estables.
Recuerda que los enlaces triples son los más reactivos debido a su menor fuerza de atracción.
Recuerda cada elemento debe compartir 2 electrones para formar el doble enlace.
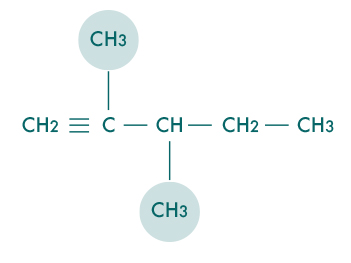
Recuerda que las estructuras ramificadas presentan otras cadenas o grupos en algunos de sus carbonos.
Recuerda que la estructura tetraédrica del carbono se debe a que tiene 4 electrones de valencia y por lo tanto puede formar 4 enlaces covalentes.